近年来兴起的以PD-1/PD-L1抑制剂为典型代表的免疫检查点阻断疗法在肿瘤治疗中取得重要进展。然而,由于抗肿瘤免疫调控的个体异质性和高度复杂性,目前批准的免疫检查点抑制剂只对少部分患者有效,在绝大多数未经挑选的实体瘤中,单独使用PD-1或PD-L1抑制剂的有效率只有10%-30%,相关疗法普遍存在部分患者响应率低、治疗场景受限等瓶颈。深入揭示并阐明相关肿瘤免疫检查点分子调控机制和肿瘤免疫逃逸机制,或将为肿瘤病患带来新的希望。
蛋白翻译后修饰是决定其功能多样性与维持细胞活动调控精准性与复杂性的重要细胞生物学事件之一。作为肿瘤免疫逃逸的核心节点分子,PD-L1等免疫检查点的糖基化、泛素化、棕榈酰化、乙酰化、磷酸化等翻译后修饰在其成熟、降解、转位中发挥重要调控作用,深入寻找免疫检查点分子翻译后修饰调节因子及阐明其具体调控机制或将为肿瘤免疫治疗提供新靶点和新策略,具有重要科学研究意义与临床转化价值。

近日,浙江大学上海高等研究院周如鸿教授,浙江大学林爱福教授、周天华教授,加州大学欧文分校王闻起教授和西湖大学生命科学学院李旭教授等多团队联合在《Nature Communications》发表题为“Promoting anti-tumor immunity by targeting TMUB1, a modulator of PD-L1 polyubiquitination and glycosylation”的研究论文,揭示了靶向PD-L1翻译后修饰调节因子TMUB1可有效逆转抑制性肿瘤免疫微环境,相关免疫治疗联合靶向策略开发具有重要临床转化价值。
研究人员通过对临床大数据深度调研分析,发现糖基化、泛素化等重要翻译后修饰通路在PD-L1高表达的肿瘤患者中高度富集,并与PD-1/PD-L1单抗响应率低显著关联。进一步发现PD-L1在肿瘤组织中具有更高的翻译后修饰水平,暗示深入揭示PD-L1翻译后修饰调控机制或为相关免疫疗法提供潜在靶向策略。基于上述前期发现,团队结合质谱和生信分析成功筛选到一批PD-L1候选互作分子,其中作为内质网膜蛋白质量控制元件的跨膜和泛素样结构域蛋白1(TMUB1)在胃癌、乳腺癌等肿瘤组织中高表达,并与CD8+ T细胞浸润高度显著负相关,暗示其在PD-L1介导的肿瘤免疫逃逸中具有潜在调控功能。深入机制研究证实TMUB1在PD-L1的多个翻译后修饰调控中发挥重要功能。一方面,内质网定位的TMUB1通过与E3泛素连接酶HUWE1竞争性结合PD-L1,极大削弱PD-L1的泛素化途径降解,继而增强PD-L1的蛋白稳定性;另一方面,TMUB1通过招募相关糖基转移酶,促进PD-L1糖基化修饰、成熟、细胞膜转位和肿瘤微环境调控功能发挥,最终导致肿瘤实现免疫逃逸。
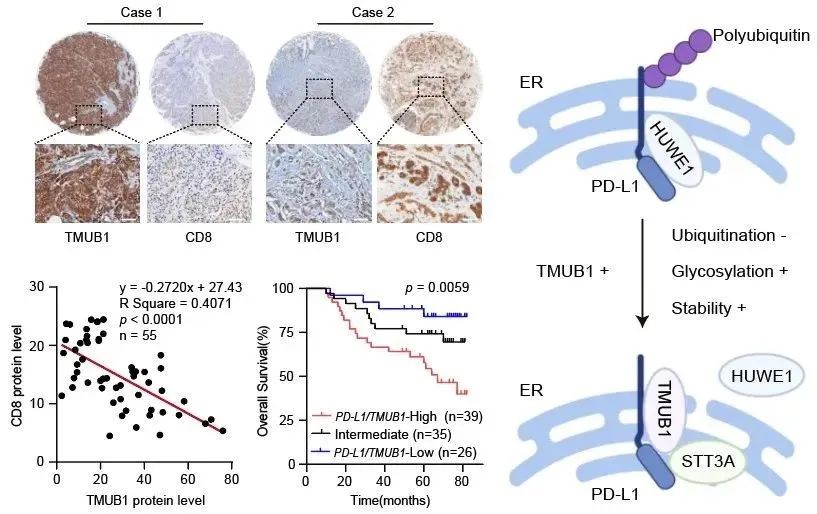
图1 乳腺癌患者临床分析TMUB1及其参与PD-L1翻译后修饰核心机制示意图
上述TMUB1对PD-L1翻译后修饰调控机制的研究发现暗示TMUB1作为肿瘤免疫治疗联合靶点的临床潜力。借助多团队交叉优势开展联合攻关,通过计算结构模拟、结合区段筛选、多肽类前体药物分子设计及体内外系列功能验证,研究人员设计开发了一款靶向多肽PTPR,通过抑制TMUB1与PD-L1的结合,成功阻断TMUB1对PD-L1的多重翻译后修饰调控,在胃癌、乳腺癌等多种荷瘤小鼠模型取得了显著抑制肿瘤生长疗效,并验证了该多肽类抑制剂的体内生物安全性。进一步,开展与αCTLA4等免疫检查点分子单抗药物联合,成功逆转了抑制性肿瘤免疫微环境,极大增强了细胞毒性T细胞的浸润和对肿瘤细胞的特异性杀伤,最终实现肿瘤抑制疗效。
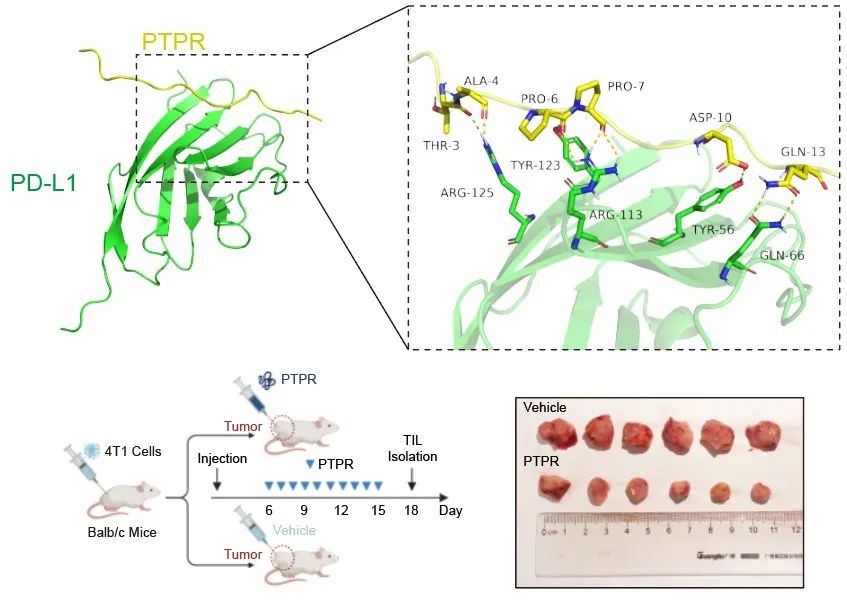
图2 靶向肽PTPR的结构对接模拟与在4T1荷瘤小鼠模型中取得的疗效
综上,该研究揭示了PD-L1翻译后修饰的调控机制及相关肿瘤免疫逃逸的分子机理,临床前证据表明TMUB1可作为免疫治疗的可靠联合靶点,开发的多肽类前体药物分子,进一步证明靶向PD-L1翻译后修饰调控分子策略具有重要临床转化价值。
原文链接可参见https://www.nature.com/articles/s41467-022-34346-x,该工作得到了科技部重点研发计划、国家自然科学基金、浙江大学上海高等研究院繁星科学基金等资助。
转载于:浙江大学生命科学学院


